Kapittelet ble revidert på obstetrisk guidelinemøte april -22. Det er vedtatt å foreta et oppdatert systematisk litteratursøk når det gjelder opplæring i CTG. Avsnittet vil bli revidert når dette arbeidet er fullført.
Gjennomgått på hurtigrevisjon april -23
Anbefalinger
- Det anbefales intermitterende auskultasjon for lavrisiko graviditeter og fødsler. (Ia)
- Det anbefales modifisert FIGO 1987 CTG klassifikasjon. (III)
- Det anbefales kontinuerlig CTG med STAN (Ia) eller foster skalpblodprøve for risikograviditeter og fødsler.
- Det anbefales sen avnavling etter fødsel av både premature og terminfødte barn. (Ia)
- Det anbefales ikke melking av navlesnoren hos premature barn under uke 28 som en erstatning for sen avnavling. (Ib)
- Det foreslås å ta syre-base fra navlesnor fra hele fødepopulasjonen. (III)
- Det anbefales opplæring med sertifisering, kontinuerlig oppfølging og undervisning i fødselsovervåkning. (IV)
Søkestrategi
Litteratursøk er utført i Pubmed, McMaster Plus og Cochrane databasen. I tillegg er RCOG guidelines og ACOG anbefalinger benyttet. Siste søk utført februar 2022.
Fosterovervåkning under fødsel
Målsettingen med overvåkning av fosteret under fødselen (intrapartum), er å oppdage de fostre som kan få alvorlige skader eller dø på grunn av oksygenmangel og gjøre tiltak for å unngå dette. Som en videre konsekvens vil den nevrologiske langtidsmorbiditeten og den perinatale mortaliteten relatert til intrapartal fosterasfyksi reduseres.
Internasjonal konsensus definerer en hypoksisk hendelse under fødsel som årsak til cerebral parese (CP) med følgende kriterier.(1, 2)
Hovedkriterier
1. Metabolsk acidose i navlearterie eller tidlig neonatal prøve som viser : pH< 7,00 og BD≥12 mmol/L
2. Tidlige tegn på alvorlig eller moderat neonatal encefalopati hos barn >34 uker
3. CP av typen spastisk kvadriplegi eller av dyskinetisk type
4. Eksklusjon av andre identifiserbare årsaker til CP, f.eks. Koagulasjon eller genetiske forstyrrelser, infeksjon, feber under fødsel, antepartum blødning, prematuritet, intrauterin vekstrestriksjon, stram navlesnor rundt halsen, komplikasjoner fra flerling svangerskap.
Tilleggskriterier som indikerer en intrapartum hendelse som årsak, men som i seg selv er uspesifikke
5. En hendelse, tilstrekkelig til å forårsake plutselig alvorlig hypoksi hos friskt foster, f.eks. navlesnorprolaps, blødning i svangerskapet, uterus ruptur
6. Plutselig vedvarende bradykardi fra den hendelsen
7. Apgar skår <4 mer enn 5 minutt
8. Tegn til påvirkning av flere organer i neonatalperioden
9. Tidlig avvik ved neuro-radiologisk undersøkelse av hjernen (innen 5 dager) med ødema og intrakraniell blødning
Hovedkriterier 1-3 skal være til stede for at en intrapartum hendelse er årsak til CP. Om det ikke finnes blodgassdata som viser metabolsk acidose, kan en ikke slå fast at intrapartum asfyksi er årsak til CP.
Det er flere studier som viser at lav pH eller metabolsk acidose i navlesnor øker risiko for langtids morbiditet. En populasjonsstudie fra Finland, med over 1 million barn til termin, viste at alvorlig acidemi med navlesnor pH <7,00 samt navlesnors-pH mellom 7,00 og 7,10 øker risikoen for nevrologiske sekveler som CP, epilepsi, intellektuelle og sensoriske defekter.(3)
Metoder for intrapartum fosterovervåking
Valg av metode avhenger av risikofaktorer hos mor og barn. Det er viktig å vurdere fødselsforløpet fortløpende og tilpasse overvåkningsmetoden. Den må oppgraderes fra lav-risiko til risikogruppe når kliniske forhold tilsier det. Det kan være protrahert forløp, misfarget fostervann, mistanke om forandring i fosterlyd (for eksempel frekvens) ved intermitterende auskultasjon, blødning, feber, behov for stimulering med oxytocin etc.
1. Intermitterende auskultasjon
For friske kvinner med ukompliserte svangerskap (lav risiko) anbefales overvåkning med intermitterende auskultasjon i aktiv fødsel. For evidens se avsnitt for intrapartum CTG.
Det finnes ikke god dokumentasjon for anbefalt hyppighet og varighet av intermitterende auskultasjon, dagens praksis er erfarings basert.(4) Evidens for etterlevelse av intermitterende auskultasjon mangler.
Det foreslås at intermitterende auskultasjon gjøres under og etter en kontraksjon og i minst 60 sekund ved hjelp av jordmor stetoskop eller Doppler.
- I åpningsfasen av aktiv fødsel: hvert 15-30. min
- I utdrivningsfasen: under og etter hver ri, minst hvert 5. min
Denne type overvåking er også aktuell ved ekstrem prematuritet.
Aktiv trykketid påfører ekstra risiko for fosteret, og kontinuerlig CTG-overvåkning vurderes hvis fosteret ikke er forløst etter 30 min aktiv trykking.(5)
2. Intrapartum kontinuerlig kardiotokografi (CTG)
CTG registrerer både rier og fosterhjertefrekvens og utføres som regel kontinuerlig i fødsel.
Metaanalysen av 13 RKS med totalt 37 000 fødsler fra Cochrane har undersøkt bruk av kontinuerlig CTG versus intermitterende auskultasjon. Den viste at intrapartum CTG-overvåking ikke førte til en reduksjon i perinatal mortalitet eller forekomst av CP. Den viste derimot signifikant færre barn med neonatale kramper og en signifikant økning i keisersnitt og operative vaginale forløsninger ved bruk av kontinuerlig CTG.(6)
Det bør understrekes at de studiene som ligger til grunn for analysen ikke hadde adekvat størrelse for å besvare om CTG gir redusert mortalitet. Studiene i Cochrane review fyller ikke dagens kvalitetskrav for RKS. Flere av de inkluderte studiene har multiple mangler: redegjør ikke om kontaminering mellom gruppene, beskriver ikke randomiseringsprosessen (allocation), eller randomiseringen er ikke gjort på en adekvat måte, blinding er ikke beskrevet, protokoll ikke publisert før studiestart.
Mange av studiene har inkludert alle typer fødsler; premature, tvillinger og kvinner med tidligere keisersnitt, dvs disse studiene har ikke forsket på lavrisikokvinner. «Lavrisikokvinner/-gravide» var ikke et begrep som var i bruk denne gangen.
Keisersnittfrekvens i hele populasjonen var 3,6%, noe som bekrefter at fødselshjelpen har endret seg kraftig siden den gangen, og studiene er utgått på dato.
Computerbasert analyse av intrapartum CTG er en relativt ny, lovende teknologi, med sikte på å øke objektiviteten ved tolkning av CTG mønstret assosiert med fosterhypoksi. Tre RKS inkluderte 54.492 fødsler, sammenlignet visuell analyse med bruk av computerbasert CTG overvåking under fødsel. Det var ingen signifikant reduksjon av metabolsk acidose eller av obstetriske inngrep.(7)
CTG-prosedyre og indikasjoner
Overvåkningen gjøres med ekstern med Doppler probe eller intern CTG med skalpelektrode, som analyserer R-R intervall i føtal elektrokardiogram (EKG). Når ekstern CTG er påkoblet, bør mors puls telles og dokumenteres manuelt eller med pulsoksymeter. Intern registrering med skalpelektrode gir mindre risiko for forveksling mellom mors og fosters puls.(8) I tillegg gir det en bedre teknisk registrering, og bør foretrekkes etter vannavgang eller utført amniotomi. Skalpelektrode skal ikke brukes når kvinnen er smittebærende (antigen positiv) med Hepatitt B og C, og HIV. Der det er ukjent smittestatus, bør kvinnen behandles som smittebærer inntil svar foreligger. Ved hemofili eller en annen blødningstilstand hos fosteret (som trombocytopeni etc), må nytten av skalpelektrode veies mot mulig blødningsfare.
Riaktiviteten registreres også, vanligvis ved å bruke ekstern TOCO-dynamometer. Det eksisterer andre metoder for riregistrering som intrauterin måling med trykkateter og ekstern elektrohysterografi. Elektrohysterografi registrerer rier bedre en TOCO-dynamometer hos både normalvektige og overvektige kvinner. (9)
For å kunne klassifisere CTG bør registreringen pågå i minimum 20 min, med mindre det er preterminalt mønster.
Kontinuerlig CTG bør være basis overvåking/screening ved risikofødsler (Tabell 1), der det finnes risikofaktorer i svangerskap og fødsel som er assosiert med økt forekomst av CP, perinatal død eller neonatal encefalopati.

CTG tolkning
Det anbefales intrapartum CTG-tolking etter forenklete retningslinjer fra Internasjonal Føderasjon i Gynekologi og Obstetrikk (FIGO) (10) (Tabell 2).
Hvorfor fortsette med FIGO klassifikasjon fra 1987?
I 2015 publiserte FIGO ny anbefaling for CTG inndeling basert på internasjonal konsensus. Det ble blant annet endret den øvre grensen for frekvens til 160/min, men man anerkjente delte meninger i konsensusgruppen. Det er holdepunkter for at FIGO klassifikasjonen fra 2015 har lavere sensitivitet å oppdage acidose hos fosteret. (11) Det kan skyldes blant annet at den reviderte FIGO klassifikasjonen fra 2015 ikke tar høyde for økt nyfødtmorbiditet blant fostre med en basalfrekvens mellom 150-160 slag/min, sammenlignet med kontrollgruppen (110-150 slag/min).(12)
Den modifiserte FIGO 1987 klassifikasjon av CTG har vært brukt i store RKS (13-16) og observasjonsstudier om fosterovervåkning med godt utfall (17, 18) og er godt innarbeidet på alle norske fødeavdelinger. Det er en stadig synkende perinatal mortalitet og samtidig stabil intervensjonsfrekvens (keisersnitt, tang, vakuum) blant fødende i Norge. I tillegg viste publiserte norske data reduksjon i forekomsten av CP, spesielt spastisk CP, som er den type CP som oftest er relatert til hypoksisk skade under fødsel.(19)
Inntil nye robuste studier viser ny evidens, anbefales fortsatt bruk av modifisert FIGO 1987 (Tabell 2)
CTG deles i 4 klasser
1. Normal
2. Avvikende
3. Patologisk
4. Preterminal

Kommentarer til modifisert FIGO klassifikasjon:
Kombinasjon av faktorer: To eller flere avvikende parametere gir en patologisk CTG.
Fravær av akselerasjoner definerer IKKE en intrapartum CTG som avvikende eller patologisk.
Basalfrekvens: Utfra tilgjengelig litteratur hvor CTG var analysert med computerbasert teknikk er gjennomsnittlig basalfrekvens ved termin 135 slag/min og 95 percentil ligger ved 152 slag/min.(20, 21) Det betyr at 5 av 100 friske fostre med normalt fødselsutfall vil ha en basalfrekvens over 152 slag/min.(21)
For å skille normalvariasjon i basalfrekvens fra patologi er det best å sammenlikne fosteret med seg selv, dvs. bruke det som sin egen kontroll. En vurdering av fosterets basalfrekvens før fødsel (helsekort for gravide) og ved innkomst anbefales. En vedvarende endring av frekvens over tid bør tillegges vekt og kan være mer betydningsfullt enn den absolutte frekvensverdien. En økning av basalfrekvensen er uttrykk for en aktivering av det sympatiske nervesystemet i forbindelse med en pågående hypoksi eller respons på økt temperatur hos mor.
Økt variabilitet: Flere studier (22-24) har vist en sammenheng mellom varighet av økt variabilitet og risiko for acidose og nyfødt morbiditet. På denne bakgrunnen er det definert tidsintervaller, som nå er inkorporert i Tabell 2.
Klinisk retningslinje for CTG tolkning kan lastes ned her: Lenke
Oppfølging av CTG tolkning
Ved evaluering av CTG og planlegging av den videre håndtering av fødselen, må hele den kliniske fødselssituasjonen vurderes. Både jordmor og lege som er involvert i fødsel bør regelmessig klassifisere CTG-mønster og dokumentere dette, samt tiltak og videre plan.
Intrapartum-CTG gir tilstrekkelig informasjon dersom CTG klassifiseres som normalt (ingen hypoksi) eller preterminalt (hypoksi).
Avvikende og patologisk CTG kan forekomme hos ikke-hypoksiske og hypoksiske foster. Man bør da skaffe tilleggsinformasjon: reaktivitets tegn (akselerasjon) ved vaginal eksplorasjon (25, 26) eller bruke tilleggs metoder som skalpblodprøver eller ST- analyse.
Ved patologisk CTG kontakter jordmor lege for vurdering, tiltak og videre plan dokumenteres. CTG og tiltak vurderes fortløpende. Oppfølging av patologisk CTG gjøres i tett samarbeid mellom jordmor og lege.
Ved patologisk CTG i trykkefasen, bør lege varsles og etter vurdering følge utviklingen av CTG fortløpende inntil fødsel.
Fysiologiske tiltak for intrauterin resuscitering
Når fosterhypoksi mistenkes, er det nødvendig med tiltak for å unngå uønskede neonatal utfall.
Mulige fysiologiske tiltak kan være å stoppe oksytocin, gi ridempende medikamenter hvis hyppige rier eller hyperton uterus. Det bør hovedsakelig brukes Atosiban 6,75 mg(0,9ml) i.v. som ridempende middel. Den kan injiseres over 1 minutt. Atosiban er oksytocinreseptor antagonist, og gitt i denne doseringen er halveringstid ca 15 minutter. Kan repeteres.
En kan gi i.v. væske som NaCl eller Ringer til mor for re-hydrering (anbefales 250ml/t), stillingsendring eller febernedsettende hvis feber (se kapittel «Feber under fødsel og chorioamnionitt»).
Amnioninfusjon er et tiltak som kan gjøres ved f. eks. oligohydramnion og variable deselerasjoner. Det vil gjerne gå mer enn 20 min før en kan forvente effekt og regnes ikke som et tiltak ved truende asfyksi som tilsier snarlig forløsning.(27)
I løpet av trykketiden kan aktiv trykking bidra til redusert placenta perfusjon og resultere i fosterhypoksi. Ved forverring av CTG under trykking bør mor instrueres i å slutte aktiv trykking (for eksempel puste gjennom ri i 10 minutter), og/eller skifte til passiv trykking med en åpen glottis.
Bruk av medikamenter og påvirkning av CTG-mønster
- Tidligere studier viste at steroider (bruk for lungemodning) gir nedsatt variabilitet opp til 72 timer etter avsluttet steroidbehandling.(28) Den nyeste og største studien fant kun et lite fall (innenfor normalvariasjonen) etter 48-71h: unormalt lave verdier bør derfor vurderes som et tegn på foster hypoksi.(29)
- Magnesiumdrypp, ß-blokker, opioide analgetika kan gi nedsatt variabilitet.(30, 31)
- ß-reseptoragonist kan gi takykardi.(32)
- Opioide analgetika kan gi et ”pseudosinusoidalt” mønster. Samme mønster er observert hvis fosteret sutter på tommel. Pseudosinusoidale mønster vil, i motsetning til de sinusoidale mønstrene, være midlertidig og alltid ha perioder med normal, reaktiv CTG.(33)
CTG ved prematuritet (< 30-32 uker)
Registrering kan være teknisk vanskelig, men anbefales utført når barnet antas å ville være levedyktig ved fødsel. CTG-mønsteret bedømmes etter de vanlige kriterier. Viktig å vite at
- Akselerasjoner defineres som 10 slags økning som varer i 10 sekunder
- Deselerasjoner defineres som 10 slags tap som varer i 10 sekunder
- Variabiliteten kan være redusert uten at det foreligge hypoksi
- Basalfrekvensen er høyere (inntil 160 slag/min) jo kortere svangerskapet er kommet (20)
Hvordan vurdere utviklingen av hypoksi?
Longitudinale evalueringer av CTG bør gjennomføres for å forstå utviklingen, erkjenne en forverring og avgjøre behovet for tiltak. CTG-mønstre under fødsel kan raskt gå fra normal til patologisk eller preterminal ved akutte hendelser som placentaløsning, uterusruptur, blødning fra vasa previa eller navlesnorprolaps.
Det er imidlertid mer vanlig med gradvis utvikling av hypoksi i løpet av noen få timer. Fra en normal CTG utvikles ofte en endring av CTG-mønstre med sporadiske variable deselerasjoner, korte perioder med økt variabilitet, videre økt hyppighet av deselerasjoner, gradvis frekvensøkning med hyppige episoder av tachykardi eller kontinuerlig tachykardi, redusert variabilitet mellom og under deselerasjoner, og til slutt bradykardi.
Nylige studier tyder på at totalt deselerasjonsareal er bedre enn andre CTG mønstre for å predikere acidemi definert som navlearterie pH <7,10. Kombinert med tachykardi er dette forbundet med en signifikant økt risiko for neonatal morbiditet.(34)
3. Fosterskalpblodanalyse
Ved mistanke om fosterhypoksi under fødsel (avvikende/patologisk CTG), kan fosterskalpblodanalyse utføres for å få tilleggsopplysninger om tilstanden til fosteret. Metoden ble introdusert på 1960-tallet, og er basert på pH-analyse av fosterskalpblod.(35)
I den senere tid er det utviklet ”bed-side tests” for å måle laktat i fosterskalpblod. Ved måling av skalp laktat trengs mindre blod enn ved skalp pH. Dette medfører raskere svar og mulighet for rask gjentakelse. Metodene er likeverdige.
Evidens for intrapartum-CTG + skalpblodprøve
Det fins en RKS fra 1979 med totalt 690 kvinner i fødsel som sammenlignet CTG versus CTG + skalp pH. (36) Nylig ble det gjennomført en mindre RKS, som sammenlignet CTG med CTG og laktat måling.(37) Begge fant ingen forskjell i neonatalt utfall eller bruk av keisersnitt mellom de to metodene, men studiene hadde ikke styrke for å besvare disse spørsmål.
Det foreligger to RKS som sammenligner skalp-laktat versus skalp pH.(38, 39) Den største av de RKS som målte skalp-laktat (n=1496) versus skalp pH (n=1496), fant ikke noen signifikant forskjell verken i moderat acidemi eller metabolsk acidose i navlesnor.(39) Forekomst av metabolsk acidoserate var 3,2 % i skalp-laktatgruppen og 3,6 % i pH-gruppen (RR 0,91, 95 % CI 0,61-1,36). Det var signifikant forskjell i antallet mislykkete forsøk med skalp pH versus skalp-laktat. Studien viste også at 13 av 45 kasus som endte med metabolsk acidose hadde normal skalp pH eller skalp-laktat 60 min før fødsel. Dette understrekker problemet med intermittent evaluering i siste delen av fødsel.
En nylig studie publiserte referanseverdier av skalp-laktat under andre stadiet av fødsel hos dem som hadde normal CTG og 5 min Apgar score ≥ 9, og fant et intervall fra 1,1 til 5,2 mmol/l, median 2,5 mmol/L målt med Lactate Pro ä. De fant i gjennomsnitt en økning i skalp- laktat på 1,5 mmol/time under trykking.(40)
Fosterskalpprøve - prosedyre
Hvis det foreligger avvikende eller patologisk CTG (og STAN ikke brukes), bør det initialt tas skalpprøve. Hvor hyppig prøven bør gjentas er avhengig av verdien og CTG-mønsteret. Hvis patologisk CTG og normal skalp-laktat bør ny laktatprøve tas innen 60 min. Analysesvar vurderes sammen med CTG-forandringer, framgang i fødselen og annen klinisk informasjon.
Dersom det er langvarig bradykardi, eller rask forverring av en patologisk CTG, bør en ikke bruke tiden på blodprøvetaking og heller forløse.
Ulemper med metoden:
- Den er invasiv
- Den gir ikke kontinuerlig informasjon, dette medfører ofte behov for gjentatte prøver
- Selv med klar protokoll, blir det tatt prøver uten indikasjon og samtidig tas ikke prøver når det er indikasjon.(41) Det finnes ingen testet protokoll som gir anbefaling når, hvor ofte og maksimalt antall skalpblodprøver som bør tas under en fødsel
- Den er tidskrevende (42)
Tolking av analyseverdier
Referanseverdier er avhengig av benyttet måleinstrument (Tabell 3).
Tabell 3 Måling av skalp-laktat (StatStripLaktat StatStripXpress (43, 44))

Lege/jordmor bør dokumentere når skalpblodprøven er tatt, verdien av denne og videre plan.
Ved truende asfyksi bør barnet fødes innen 20 min.
Kontraindikasjoner mot skalpblodprøver er: maternell infeksjoner som: HIV, hepatitt og risiko for blødningstendens hos fosteret (hemofili, trombocytopeni).
Tilblanding av fostervann vil føre til falsk forhøyete laktatverdier, og kontroll av målt forhøyet laktat med ny prøve kan være hjelpsom.
4. CTG + ST-analyse av foster-EKG ”STAN”
STAN-teknologien er basert på automatisk evaluering av endringer i ST-intervallet i foster EKG. Overvåking med automatisk analyse av fosterets EKG i tillegg til CTG, øker spesifisiteten av overvåkingen, det vil si at en får bedre tolking av unormale CTG-mønstre. Siden det brukes intern elektrode, må fosterhinner være brutt.
Fysiologiske mekanismene bak en ST-forandringer.
ST-intervallet i EKG representerer fasen av ventrikulær repolarisering, en energikrevende prosess som er følsom for hypoksi. ST-elevasjon oppstår som et spesifikt tegn på hjertehypoksi, noe som fører til en kjemoreceptor mediert adrenalinbølge, og β-adrenoceptor-mediert anaerob metabolisme med myokardial glykogenolyse. I STAN sammenheng heter de basislinje og episodiske hendelser.
Tilstedeværelsen av en depresjon i ST-segmentet kan skyldes myokard ischemi, men er også forbundet med en reduksjon i myokard ytelse. Dermed kan i utgangspunktet alle faktorer som påvirker myokardveggenes ytelse, for eksempel prematuritet, infeksjoner, feber, myokarddystrofi og hjertesvikt, resultere i ST depresjoner. I STAN sammenheng heter de bifasiske hendelser.
Evidens for intrapartum CTG + ST-analyse av foster-EKG
Sju RKS som evaluerer STAN-teknologien, involvert 26,683 kvinner, er publisert. Seks av disse forsøkene sammenlignet CTG alene med STAN, med mulighet for skalpblodprøver i begge forsøksgrupper. En RKS brukte ikke skalpblodprøver og har annerledes CTG klassifisering enn de øvrige fem hadde. Seks RKS har blitt evaluert i flere metaanalyser, som alle har vist en reduksjon av behovet for skalpblodprøver, og en reduksjon i vaginale operative forløsninger når STAN metoden brukes. Det er tilsynelatende motstridende bevis på om bruken av STAN-teknologi reduserer forekomst av metabolsk acidose. Dessverre brukte ikke alle metaanalyser reviderte navlesnor syrebasedata fra RKS som var publiserte, heller ikke lik metodologi for beregning av Base Deficit (BD) i analysen av syrebaser fra navlesnor. Når statistikken er basert på korrekte data, reduserer STAN metoden hyppigheten av metabolsk acidose med 36% (relativ reduksjon) og 0.25% (absolutt reduksjon). (45, 46)
Flere store observasjonsstudier med mer enn 50 000 fødsler utført i løpet av de siste to tiårene har også konsekvent vist at bruken av STAN-metoden er forbundet med en reduksjon av metabolsk acidose og neonatal morbiditet.(17, 47)
Prosedyre med STAN-overvåking
STAN-systemet analyserer automatisk ST-endringene i foster-EKG slik at en får informasjon om det foreligger T/QRS-basislinjestigning (ST-elevasjon) eller bifasiske ST (ST-senkning). En T/QRS-kvote angis med et kryss i registeringen. Et kryss representerer 30 pulsasjoner hvor apparatet regner ut gjennomsnittlig T/QRS-kvote.
T/QRS-basislinjestigning kan være
- Kortvarige (innen 10 min): Episodiske T/QRS stigninger
- Langvarige (fra og med 10 min i tre timer tilbake): Basislinje T/QRS stigninger
Bifasiske ST-hendelser
- ST-depresjon er komponenten av ST-segmentet under EKG basislinje som enten skjærer EKG basislinje og er merket under et kryss som tall 2 eller er under EKG basislinje og er merket under et kryss som tall 3.
En bifasisk hendelse inneholder tre påfølgende (eller maksimum en uten) kryss som er merket 2 eller 3 (Figur 1)
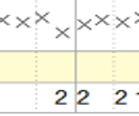
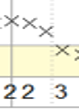
Figur 1: Eksempler på signifikant bifasisk hendelse
Antall bifasiske hendelser vil fremkomme på registreringen og i hendelsesloggen. Bifasiske hendelser bør sees i lys av aktuelt CTG (siste 20-30 minutter).
Vilkår for å bruke STAN-overvåkning er
- Risiko svangerskap og fødsel med gestasjonsalder >36 uker
- Fostervannet må ha gått spontant eller det er gjort amniotomi
- Ingen kontraindikasjon for skalpelektrode (mor med hepatitt B og C, HIV)
- Fødselen er i åpningsstadiet, eller senest i 2. stadium og helst før start av trykking
Ved starten av ST-analyse
- Klassifiser CTG i en av de 4 klasser
- Sjekk om fosteret er reaktivt (akselerasjon ved tilkobling av skalpelektrode/palpasjon)
- Sjekk signalkvalitet
- Kontroller at foster-EKG ser normalt ut (se signalfeltet EKG-komplekser)
- Sjekk loggen for hvilket tidspunkt basislinje T/QRS er bestemt
- Sørg for god ri-registrering
Hvilke ST-hendelser som krever tiltak eller forløsning fremkommer i tabell 4.
Tabell 4
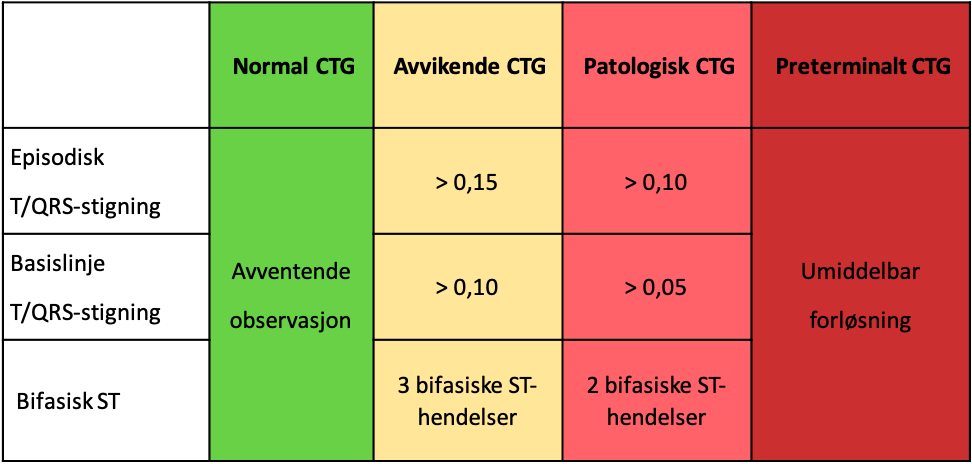
*Om CTG er normalt: se bort fra eventuelle ST-hendelser.
*Om CTG er preterminalt: Forløs umiddelbart, mer informasjon trengs ikke.
*Om CTG er avvikende eller patologisk, bruk retningslinjer for ST-analyse.
Klassifikasjon av CTG-mønsteret bør regelmessig dokumenters av jordmor og lege. Hvis signifikante ST- hendelser forekommer sammen med avvikende/patologisk CTG, bør også typen av tiltak dokumenteres.
Om retningslinjene for CTG + ST tilsier tiltak i åpningsfasen: Gjør enten målrettede fysiologiske tiltak som kan behandle årsaken til CTG-endringene (se fysiologiske tiltak).
Fysiologisk tiltak bør føre til forbedring av CTG relativt snarlig (ca. 20 min), eller vurdere forløsning. Forløs innen ca. 20 min dersom det ikke finnes målrettede tiltak som kan endre CTG.
Indikasjon for tiltak eller forløsning:
Patologisk CTG uten ST-hendelser
- Åpningstid: STAN-retningslinjer
- Hvis patologisk CTG i starten av andre stadium (ved 10 cm åpning) uten ST-hendelse, bør barnet bli født innen ca. 90 min, og en bør starte forløsning etter ca. 60 min.
- Preterminal CTG er det alltid indisert umiddelbar forløsning, med eller uten ST-hendelse
Avvikende/patologisk CTG med ST-hendelse
- Åpningstid: ca. 20 minutter: Fysiologisk tiltak bør forbedre CTG innen ca. 20 min, hvis ikke CTG bedrer seg foretas forløsning.
- Full åpning (10 cm): Forløsning innen ca. 20 min. Fysiologiske tiltak kan prøves først, dersom tiltaket er tydelig målrettet og man kan forvente snarlig bedring av CTG. Vurder forløsning fortløpende.
- I trykketiden: Umiddelbar forløsning
- Preterminal CTG i åpningsfasen og utdrivningsfasen: Umiddelbar forløsning
Tid
Foreligger forløsningsindikasjon på grunn av truende asfyksi - forløs raskt. STAN metoden kan brukes på fødeavdelinger som har god nok beredskap til å utføre operativ forløsning (keisersnitt) innen 20 min.
Det bør være lokale prosedyrer som sikrer at det dokumenteres klassifisering av CTG/STAN-registreringer.
Avdelingene bør ha en strategi for langtidslagring av CTG/STAN-registreringer. Dessuten bør alle fødeinstitusjoner ha regelmessig undervisning om elektronisk fosterovervåking for å redusere faren for feiltolking.
Viktige moment ved bruk av ST-analyse
Det er viktig å koble pasienten til STAN-overvåking tidlig i fødselsforløpet, før fosteret har redusert eller brukt opp ressurser under hypoksiutviklingen. Et foster som har vært utsatt for hypoksi viser mindre utalte reaksjoner ved ny tilkommet hypoksiepisode, de har nedsatt evne til å forsvare seg.
- Ved patologisk CTG og normal ST, ved starten av registrering: Obs. usikker ressursstatus hos fosteret. Søk mulige tilleggsopplysninger (sjekk for reaktivitet i form av akselerasjon ved palpasjon av fosterhodet, eventuelt ta skalpprøve). Man kan koble på STAN selv om CTG er patologisk ved oppstart, men på grunn av usikker ressurs status hos fosteret kan en ikke være sikker på å få en ST-hendelse. Tett oppfølging anbefales ut fra CTG-forandringer. Hvis signifikant ST-melding tilkommer bør en ikke forvente at det kommer flere, og ut fra klinikken bør en planlegge forløsningen.
- Ved forverring av et patologisk CTG-mønster til et annet patologisk CTG-mønster, uten ST-hendelser anbefales tett oppfølging. Pass spesielt på om variabiliteten reduseres ytterligere. Det er alltid vanskeligere å se noe som forsvinner enn noe som oppstår, derfor er det viktig å kommunisere med flere kollegaer for ikke å overse overgang til preterminal CTG uten ST-hendelse
- Feber hos mor. En kasuskontrollstudie har sett på bruken av STAN hos pasienter med feber, versus uten feber. Det var ingen forskjell mellom gruppene. Man anbefaler å bruke ST-analyse hos kvinner med feber, etter vanlige STAN-retningslinjer.(48)
- Ved mistanke om klinisk chorioamnionitt er det viktig å huske at fosterets ressurser kan bli brukt opp på å forsvare seg mot pågående infeksjon/inflammasjon, og dermed kan ST-hendelse mangle. I en slik situasjon bør en være spesielt oppmerksom på tidsfaktoren, endringer i CTG-mønsteret (obs. preterminalt mønster) og fødselsforløpet. Det foreligger ingen studier som har sett på bruken av STAN i denne pasientgruppen
- Antall bifasiske ST-hendelser som skal inngå i vurderingen bør være knyttet til det aktuelle CTG-mønstret (siste 20-30 minutter).
Kliniske retningslinje for bruk av STAN og sjekkliste kan lastes ned her
Avnavling og syre-base prøver fra navlesnor
Etter fødsel foretas avnavling. Vi anbefaler sen avnavling, som ikke er til hinder for samtidig umiddelbar prøvetaking fra navlesnoren til analyse av syre-base forhold. Sistnevnte er en forutsetning for en objektiv vurdering av hypoksiforekomst under fødsel.(2)
Ved sen avnavling tilføres nyfødte mer blod fra placenta i løpet av de første minuttene etter fødselen. Sen avnavling for termin-barn resulterer i høyere jern og serum ferritinverdier.(49, 50) Nylig publiserte RKS av termin barn vurdert ved 12 måneders og fire års alder viste at de som ble avnavlet etter 3 minutter hadde bedre nevrologisk utfall sammenlignet med dem som ble avnavlet umiddelbart.(51, 52)
Hos preterme barn har sen avnavling vist å ha fordeler i form av redusert risiko for intraventrikulær blødning og død samt risiko for blodtransfusjon på grunn av anemi eller hypotensjon.(53) Melking av navlesnoren har vært sett som en erstatning til autotransfusjon og sen avnavling. En nylig presentert RKS hos premature (23-27 uker) ble stoppet for tidlig fordi armen randomisert til melking av snoren hadde en økt forekomst av hjerneblødning. Denne prosedyren anbefales derfor ikke hos barn under uke 28.(54)
Det finnes så langt ikke tilstrekkelig evidens til å anbefale resuscitering av asfyktiske barn med intakt navlesnor.(55)
Syre-baseanalyse fra navlekar er de mest objektive parametere en har til å vurdere om fosteret har vært utsatt for hypoksi under fødselen.
Nytteverdi av syre-base analyse av navlesnor er:
- Objektiv og målbar informasjon om den nyfødte var utsatt for hypoksi under fødselen, en viktig informasjon for barnelegene og foreldrene
- Svært viktig for kontinuerlig kvalitetskontroll og kvalitetssikring innenfor fødselshjelp
- Viktig i klagesaker for å avklare om skaden skyldes hypoksi under fødsel
Utførelse av syre-baseprøver ved sen avnavling (anbefalt rutine):
- Gjør klar to full hepariniserte sprøyter med spiss og propp (gjerne merket henholdsvis arterie og vene) samt tørre kompresser i god tid før fødsel
- Avtal hvem som tar prøve, vedkommende må gis tilgang til navlesnoren umiddelbart etter fødsel, snoren holdes i den ene hånden, sprøyten i den andre og navlekarene identifiseres.
- En blodprøve tas først fra navlearterie og deretter fra navlevene (minste volum varierer etter type syre-base apparat)
- Fjern spiss, fjern luft så fort som mulig, sett på kork, og deretter bland godt 10 ganger opp og ned 180 grader slik at heparin kan fordele seg i hele sprøyten. Når prøven er tatt bør den analyseres så raskt som praktisk mulig og innen 30 min.
- Det er viktig å ta prøve fra både navlearterie og navlevene
Indikasjon for umiddelbar avnavling
- Sykt barn som trenger umiddelbar hjelp fra barnelege.
- Mor med antistoffer oppdaget i svangerskapet (Rhesus eller trombocytt)
- Etter forløsning av tvilling 1 ved monokoriale tvillinger og usikker korionisitet (obs, akutt tvilling-tvilling eller placenta-tvilling transfusjon)
Prosedyre for umiddelbar avnavling/utførelse av syre–baseprøver
- Gjør klar to full hepariniserte sprøyter med spiss og propp (gjerne merket henholdsvis navlearterie og navlevene)
- Klem av navlesnoren umiddelbart med tre peanger (to til avnavling mot barnet og en mot placenta); ved relativ blodtomhet melk blod inn i den delen av snoren som clampes.
- En blodprøve tas først fra navlearterie og deretter fra navlevene (minste volum varierer etter type syre-base apparat)
- Fjern spiss, fjern luft så fort som mulig, sett på kork, og deretter bland godt 10 ganger opp og ned 180 grader slik at heparin kan fordele seg i hele sprøyten. Når prøven er tatt bør den analyseres så raskt som praktisk mulig og innen 30 min.
- Det er viktig å ta prøve fra både navlearterie og navlevene
OBS. Dersom mor er HIV-, hepatitt B- eller hepatitt C-positiv skal syre-base tas etter barnet er avnavlet for å redusere smitterisiko fra mor til barn.
Beregning av Base Deficit /Base Excess i syre-base
Bestemmelse av base deficit (BD) står sentralt i vurderingen om et foster har utviklet en metabolsk acidose ved fødsel. BD er en parameter som ikke måles direkte i blodprøvene, men som kalkuleres av syre-baseapparater ut i fra målt pH og pCO2. Det finnes ulike algoritmer for beregning og BD som vil kunne variere 1-2mmol for en gitt pH og pCO2, avhengig av hvilken algoritme som syre-baseapparatet bruker.(56, 57)
For nyfødte blir det anbefalt å beregne BD i ekstracellulærrommet (BDecf) etter Siggaard Andersens algoritme. (58) Sjekk hvilken algoritme ditt syre-baseapparat bruker for beregning av BDecf, ellers kan du finne algoritme på NGF nettsider: Lenke
Kvalitetssikring av syrebase prøver (59)
Feil under prøvetaking og analyse kan påvirke målte verdier av ph og pCO2.
For at en skal være sikker på at prøvene er separat fra navlearterie og navlevene må:
- pH være 0,02 lavere i navlearterie enn i navlevene
- pCO2 > 0,7 kPa høyere i navlearterie enn i navlevene
- pCO2 kan ikke være under 2,9 kPa
Etter at en har fått resultatene fra begge navlekarene bør det sjekkes i prosentilskjema om pCO2 ligger innen forventet område, for denne spesifikke pH verdien. Prosentilskjema er publisert.(59) Det kan lastes ned fra NGF nettsider: Lenke
Fortolkning hvis begge navlekar til stedet:

Hvis det eksisterer prøve fra kun et navlekar (sannsynligvis venen), kan en ikke være sikker på at det andre manglende navlekaret (sannsynligvis arterien) ikke viste metabolsk acidose. Hvis derimot det er prøve fra kun et navlekar som viser metabolsk acidose er denne reell uansett.
Opplæring i fødselsoveråkning
Det er kjent at tolking av CTG er subjektiv, og at det kan være lav grad av enighet mellom bedømmere, spesielt når det gjelder CTG-mønstre som kan tolkes som unormale (60). Systematisk opplæring kan føre til bedre enighet i tolking av CTG, eller mer korrekt tolking, men ikke nødvendigvis til bedre utfall (61-63).
En stor dansk kohortstudie undersøkte om implementering av et nasjonalt, tverrfaglig opplæringsprogram i tolking av CTG var assosiert med reduksjon i risiko for pH <7,00 i navlestrengsblod, apgarskår <7 etter fem minutter og hypotermibehandling. De fant ingen signifikante forskjeller i neonatale utfall. De undersøkte også om det var forskjeller i risiko for operative forløsninger, og fant en liten reduksjon i andel operative vaginale forløsninger etter at opplæringsprogrammet ble implementert (absolutt reduksjon 0,8%, relativ reduksjon 14%) (64).
En systematisk oversikt har undersøkte effekten av trening/opplæring i intrapartum CTG (65). Oversikten inkluderte 64 studier. Fem randomiserte studier fant at trening økte kunnskap, men samlet evidens var av lav kvalitet. Selv om studien ikke fant evidens som viser at trening gir bedre utfall hos mor og barn, anbefalte den lokal, tverrfaglig, team-basert utdanning i fosterovervåkning på linje med annen trening innen fødselshjelp.
Det er også i Norge bred faglig enighet om at systematisk opplæring i tolking og bruk av CTG er viktig. Arbeidsgiver har også ansvar for at ansatte som arbeider med fosterovervåking skal ha den kompetansen som kreves, og skal sørge for opplæring.
Referanser:
1. MacLennan A. A template for defining a causal relation between acute intrapartum events and cerebral palsy: international consensus statement. BMJ. 1999;319(7216):1054-9.
2. MacLennan AH, Thompson SC, Gecz J. Cerebral palsy: causes, pathways, and the role of genetic variants. Am J Obstet Gynecol. 2015;213(6):779-88.
3. Seikku L, Gissler M, Andersson S, Rahkonen P, Stefanovic V, Tikkanen M, et al. Asphyxia, Neurologic Morbidity, and Perinatal Mortality in Early-Term and Postterm Birth. Pediatrics. 2016;137(6).
4. Blix E, Maude R, Hals E, Kisa S, Karlsen E, Nohr EA, et al. Intermittent auscultation fetal monitoring during labour: A systematic scoping review to identify methods, effects, and accuracy. PLoS One. 2019;14(7):e0219573.
5. Yli BM, Kro GA, Rasmussen S, Khoury J, Noren H, Amer-Wahlin I, et al. How does the duration of active pushing in labor affect neonatal outcomes? J Perinat Med. 2011.
6. Alfirevic Z, Devane D, Gyte GM. Continuous cardiotocography (CTG) as a form of electronic fetal monitoring (EFM) for fetal assessment during labour. Cochrane Database Syst Rev. 2017;2:CD006066.
7. Campanile M, D'Alessandro P, Della Corte L, Saccone G, Tagliaferri S, Arduino B, et al. Intrapartum cardiotocography with and without computer analysis: a systematic review and meta-analysis of randomized controlled trials. J Matern Fetal Neonatal Med. 2018:1-7.
8. Neilson DR, Jr., Freeman RK, Mangan S. Signal ambiguity resulting in unexpected outcome with external fetal heart rate monitoring. Am J Obstet Gynecol. 2008;198(6):717-24.
9. Vlemminx MWC, Rabotti C, van der Hout-van der Jagt MB, Oei SG. Clinical Use of Electrohysterography During Term Labor: A Systematic Review on Diagnostic Value, Advantages, and Limitations. Obstet Gynecol Surv. 2018;73(5):303-24.
10. Rooth G, Huch A, Huch R. Guidelines for the use of fetal monitoring. Int J Gynaecol Obstet. 1987;25:159-67.
11. Olofsson P, Ekengard F, Herbst A. Time to reconsider: Have the 2015 FIGO and 2017 Swedish intrapartum cardiotocogram classifications led us from Charybdis to Scylla? Acta Obstet Gynecol Scand. 2021;100(9):1549-56.
12. Ghi T, Di Pasquo E, Dall'Asta A, Commare A, Melandri E, Casciaro A, et al. Intrapartum fetal heart rate between 150 and 160 bpm at or after 40 weeks and labor outcome. Acta Obstet Gynecol Scand. 2021;100(3):548-54.
13. Amer-Wåhlin I, Kjellmer I, Maršál K, Olofsson P, Rosén KG. Swedish randomized controlled trial of cardiotocography only versus cardiotocography plus ST analysis of fetal electrocardiogram revisited: analysis of data according to standard versus modified intention-to-treat principle. Acta Obstet Gynecol Scand. 2011;90(9):990-6.
14. Westerhuis ME, Visser GH, Moons KG, Zuithoff N, Mol BW, Kwee A. Cardiotocography plus ST analysis of fetal electrocardiogram compared with cardiotocography only for intrapartum monitoring: a randomized controlled trial. Obstet Gynecol. 2011;117(2 Pt 1):406-7.
15. Amer-Wåhlin I, Hellsten C, Noren H, Hagberg H, Herbst A, Kjellmer I, et al. Cardiotocography only versus cardiotocography plus ST analysis of fetal electrocardiogram for intrapartum fetal monitoring: a Swedish randomised controlled trial. Lancet. 2001;358(9281):534-8.
16. Westerhuis M, Visser GHA, Moons KGM, van Beek E, Benders MJ, Bijvoet SM, et al. Cardiotocography plus ST analysis of fetal electrocardiogram compared with cardiotocography only for intrapartum monitoring: a randomized controlled trial. Obstet Gynecol. 2010;115(6):1173-80.
17. Timonen S, Holmberg K. The importance of the learning process in ST analysis interpretation and its impact in improving clinical and neonatal outcomes. Am J Obstet Gynecol. 2018.
18. Kessler J, Moster D, Albrechtsen S. Intrapartum monitoring of high-risk deliveries with ST analysis of the fetal electrocardiogram: an observational study of 6010 deliveries. Acta Obstet Gynecol Scand. 2013;92(1):75-84.
19. Hollung SJ, Vik T, Lydersen S, Bakken IJ, Andersen GL. Decreasing prevalence and severity of cerebral palsy in Norway among children born 1999 to 2010 concomitant with improvements in perinatal health. Eur J Paediatr Neurol. 2018;22(5):814-21.
20. Amorim-Costa C, Costa-Santos C, Ayres-de-Campos D, Bernardes J. Longitudinal evaluation of computerized cardiotocographic parameters throughout pregnancy in normal fetuses: a prospective cohort study. Acta Obstet Gynecol Scand. 2016;95(10):1143-52.
21. Serra V, Bellver J, Moulden M, Redman CW. Computerized analysis of normal fetal heart rate pattern throughout gestation. Ultrasound Obstet Gynecol. 2009;34(1):74-9.
22. Tarvonen M, Hovi P, Sainio S, Vuorela P, Andersson S, Teramo K. Intrapartum zigzag pattern of fetal heart rate is an early sign of fetal hypoxia: A large obstetric retrospective cohort study. Acta Obstet Gynecol Scand. 2021;100(2):252-62.
23. Loussert L, Berveiller P, Magadoux A, Allouche M, Vayssiere C, Garabedian C, et al. Association between marked fetal heart rate variability and neonatal acidosis: A prospective cohort study. BJOG. 2023;130(4):407-14.
24. Gracia-Perez-Bonfils A, Vigneswaran K, Cuadras D, Chandraharan E. Does the saltatory pattern on cardiotocograph (CTG) trace really exist? The ZigZag pattern as an alternative definition and its correlation with perinatal outcomes. J Matern Fetal Neonatal Med. 2021;34(21):3537-45.
25. Skupski DW, Rosenberg CR, Eglinton GS. Intrapartum fetal stimulation tests: a meta-analysis. Obstet Gynecol. 2002;99(1):129-34.
26. Holzmann M, Wretler S, Nordstrom L. Absence of accelerations during labor is of little value in interpreting fetal heart rate patterns. Acta Obstet Gynecol Scand. 2016;95(10):1097-103.
27. Hofmeyr GJ, Lawrie TA. Amnioinfusion for potential or suspected umbilical cord compression in labour. Cochrane Database Syst Rev. 2012;1:CD000013.
28. Subtil D, Tiberghien P, Devos P, Therby D, Leclerc G, Vaast P, et al. Immediate and delayed effects of antenatal corticosteroids on fetal heart rate: a randomized trial that compares betamethasone acetate and phosphate, betamethasone phosphate, and dexamethasone. Am J Obstet Gynecol. 2003;188(2):524-31.
29. Knaven O, Ganzevoort W, de Boer M, Wolf H. Fetal heart rate variation after corticosteroids for fetal maturation. Eur J Obstet Gynecol Reprod Biol. 2017;216:38-45.
30. Duffy CR, Odibo AO, Roehl KA, Macones GA, Cahill AG. Effect of magnesium sulfate on fetal heart rate patterns in the second stage of labor. Obstet Gynecol. 2012;119(6):1129-36.
31. Jansson LM, Velez M, McConnell K, Spencer N, Tuten M, Jones HE, et al. Maternal buprenorphine treatment and fetal neurobehavioral development. Am J Obstet Gynecol. 2017;216(5):529 e1- e8.
32. Abdelhak Y, Roque H, Young BK. Terbutaline: effects on the fetal heart at term. J Perinat Med. 2011;40(1):69-71.
33. Murphy KW, Russell V, Collins A, Johnson P. The prevalence, aetiology and clinical significance of pseudo-sinusoidal fetal heart rate patterns in labour. Br J Obstet Gynaecol. 1991;98(11):1093-101.
34. Cahill AG, Tuuli MG, Stout MJ, Lopez JD, Macones GA. A prospective cohort study of fetal heart rate monitoring: deceleration area is predictive of fetal acidemia. Am J Obstet Gynecol. 2018;218(5):523 e1- e12.
35. Bretscher J, Saling E. pH values in the human fetus during labor. Am J Obstet Gynecol. 1967;97(7):906-11.
36. Haverkamp AD, Thompson HE, McFee JG, Cetrulo C. The evaluation of continuous fetal heart rate monitoring in high-risk pregnancy. Am J Obstet Gynecol. 1976;125(3):310-20.
37. East CE, Davey MA, Kamlin COF, Davis PG, Sheehan PM, Kane SC, et al. The addition of fetal scalp blood lactate measurement as an adjunct to cardiotocography to reduce caesarean sections during labour: The Flamingo randomised controlled trial. Aust N Z J Obstet Gynaecol. 2021;61(5):684-92.
38. Westgren M, Kruger K, Ek S, Grunevald C, Kublickas M, Naka K, et al. Lactate compared with pH analysis at fetal scalp blood sampling: a prospective randomised study. Br J Obstet Gynaecol. 1998;105(1):29-33.
39. Wiberg-Itzel E, Lipponer C, Norman M, Herbst A, Prebensen D, Hansson A, et al. Determination of pH or lactate in fetal scalp blood in management of intrapartum fetal distress: randomised controlled multicentre trial. BMJ. 2008;336(7656):1284-7.
40. Wiberg N, Kallen K. Fetal scalp blood lactate during second stage of labor: determination of reference values and impact of obstetrical interventions. J Matern Fetal Neonatal Med. 2017;30(5):612-7.
41. Becker J, Westerhuis M, Sterrenburg K, van den Akker E, van Beek E, Bolte A, et al. Fetal blood sampling in addition to intrapartum ST-analysis of the fetal electrocardiogram: evaluation of the recommendations in the Dutch STAN® trial. BJOG. 2011;118:1239-46.
42. Rimmer S, Roberts SA, Heazell AE. Cervical dilatation and grade of doctor affects the interval between decision and result of fetal scalp blood sampling in labour. J Matern Fetal Neonatal Med. 2016;29(16):2671-4.
43. Iorizzo L, Carlsson Y, Johansson C, Berggren R, Herbst A, Wang M, et al. Proposed cutoff for fetal scalp blood lactate in intrapartum fetal surveillance based on neonatal outcomes: a large prospective observational study. BJOG. 2022;129(4):636-46.
44. Wang M, Chua SC, Bouhadir L, Treadwell EL, Gibbs E, McGee TM. Point-of-care measurement of fetal blood lactate - Time to trust a new device. Aust N Z J Obstet Gynaecol. 2018;58(1):72-8.
45. Blix E, Brurberg KG, Reierth E, Reinar LM, Oian P. ST waveform analysis versus cardiotocography alone for intrapartum fetal monitoring: a systematic review and meta-analysis of randomized trials. Acta Obstet Gynecol Scand. 2016;95(1):16-27.
46. Vayssiere C, Ehlinger V, Paret L, Arnaud C. Is STAN monitoring associated with a significant decrease in metabolic acidosis at birth compared with cardiotocography alone? Review of the three meta-analyses that included the recent US trial. Acta Obstet Gynecol Scand. 2016;95(10):1190-1.
47. Landman A, Immink-Duijker ST, Mulder EJH, Koster MPH, Xodo S, Visser GHA, et al. Significant reduction in umbilical artery metabolic acidosis after implementation of intrapartum ST waveform analysis of the fetal electrocardiogram. Am J Obstet Gynecol. 2019;221(1):63 e1- e13.
48. Becker JH, van Rijswijk J, Versteijnen B, Evers AC, van den Akker ES, van Beek E, et al. Is intrapartum fever associated with ST-waveform changes of the fetal electrocardiogram? A retrospective cohort study. BJOG. 2012;119(11):1410-6.
49. McDonald SJ, Middleton P, Dowswell T, Morris PS. Effect of timing of umbilical cord clamping of term infants on maternal and neonatal outcomes. Cochrane Database Syst Rev. 2013(7):CD004074.
50. Andersson O, Hellstrom-Westas L, Andersson D, Domellof M. Effect of delayed versus early umbilical cord clamping on neonatal outcomes and iron status at 4 months: a randomised controlled trial. BMJ. 2011;343:d7157.
51. Andersson O, Domellof M, Andersson D, Hellstrom-Westas L. Effect of delayed vs early umbilical cord clamping on iron status and neurodevelopment at age 12 months: a randomized clinical trial. JAMA pediatrics. 2014;168(6):547-54.
52. Andersson O, Lindquist B, Lindgren M, Stjernqvist K, Domellof M, Hellstrom-Westas L. Effect of Delayed Cord Clamping on Neurodevelopment at 4 Years of Age: A Randomized Clinical Trial. JAMA pediatrics. 2015;169(7):631-8.
53. Fogarty M, Osborn DA, Askie L, Seidler AL, Hunter K, Lui K, et al. Delayed vs early umbilical cord clamping for preterm infants: a systematic review and meta-analysis. Am J Obstet Gynecol. 2018;218(1):1-18.
54. Katheria A, Reister F, Essers J, Mendler M, Hummler H, Subramaniam A, et al. Association of Umbilical Cord Milking vs Delayed Umbilical Cord Clamping With Death or Severe Intraventricular Hemorrhage Among Preterm Infants. JAMA. 2019;322(19):1877-86.
55. Katheria AC. Neonatal Resuscitation with an Intact Cord: Current and Ongoing Trials. Children (Basel). 2019;6(4).
56. Wiberg N, Kallen K, Olofsson P. Base deficit estimation in umbilical cord blood is influenced by gestational age, choice of fetal fluid compartment, and algorithm for calculation. Am J Obstet Gynecol. 2006;195(6):1651-6.
57. Mokarami P, Wiberg N, Olofsson P. An overlooked aspect on metabolic acidosis at birth: blood gas analyzers calculate base deficit differently. Acta Obstet Gynecol Scand. 2012;91(5):574-9.
58. Siggaard-Andersen O. An acid-base chart for arterial blood with normal and pathophysiological reference areas. Scand J Clin Lab Invest. 1971;27(3):239-45.
59. Kro GA, Yli BM, Rasmussen S, Noren H, Amer-Wahlin I, Saugstad OD, et al. A new tool for the validation of umbilical cord acid-base data. BJOG. 2010;117(12):1544-52.
60. Rhose S, Heinis AM, Vandenbussche F, van Drongelen J, van Dillen J. Inter- and intra-observer agreement of non-reassuring cardiotocography analysis and subsequent clinical management. Acta obstetricia et gynecologica Scandinavica. 2014;93(6):596-602.
61. Millde-Luthander C, Hogberg U, Nystrom ME, Pettersson H, Wiklund I, Grunewald C. The impact of a computer assisted learning programme on the ability to interpret cardiotochography. A before and after study. Sexual & reproductive healthcare : official journal of the Swedish Association of Midwives. 2012;3(1):37-41.
62. Pettker CM, Thung SF, Norwitz ER, Buhimschi CS, Raab CA, Copel JA, et al. Impact of a comprehensive patient safety strategy on obstetric adverse events. American journal of obstetrics and gynecology. 2009;200(5):492.e1-.e8.
63. Draycott T, Sibanda T, Owen L, Akande V, Winter C, Reading S, et al. Does training in obstetric emergencies improve neonatal outcome? BJOG: An International Journal of Obstetrics & Gynaecology. 2006;113(2):177-82.
64. Thellesen L, Bergholt T, Sorensen JL, Rosthoej S, Hvidman L, Eskenazi B, et al. The impact of a national cardiotocography education program on neonatal and maternal outcomes: A historical cohort study. Acta obstetricia et gynecologica Scandinavica. 2019;98(10):1258-67.
65. Kelly S, Redmond P, King S, Oliver-Williams C, Lame G, Liberati E, et al. Training in the use of intrapartum electronic fetal monitoring with cardiotocography: systematic review and meta-analysis. Bjog-an International Journal of Obstetrics and Gynaecology. 2021;128(9):1408-19.